碳酸二甲酯 (DMC) 是绿色无污染的化学品,具有广泛的应用前景,如用于聚合物的合成、燃料添加剂以及绿色溶剂[1, 2],因此DMC的研究受到社会广泛关注。目前DMC常用的合成方法有甲醇氧化羰基化法、尿素醇解法和酯交换法[1, 2, 3]。在这些合成路线中,由CO2和甲醇直接合成DMC是最具吸引力的合成路线。不仅因为这个反应原子经济性高、符合绿色化学的基本原则,还因为这个反应以CO2为原料可以缓解过量CO2造成的温室效应。因此这个反应是近年来的研究热点,多种催化剂被用于这个反应体系,包括有机金属化合物[4]、ZrO2[5, 6, 7]、CeO2[8, 9]和Cu基催化剂[10, 11]等。这些催化剂中,ZrO2和CeO2表现出较好的活性,催化剂表面的酸碱性被认为与催化剂的活性有关[12, 13, 14]。La等[12]将磷钨酸改性的铈钛固溶体CexTi1-xO2用于DMC的合成研究中,研究结果得出由于H3PW12O40提供的B酸位和CexTi1-xO2提供的碱性位共同作用使得H3PW12O40/Ce0.1Ti0.9O2具有较好的催化活性。Lee[13]报道了Ga改性后具有最大酸碱量的Ce0.6Zr0.4O2表现出最适宜的催化活性。
本研究通过向氧化铈中掺杂不同金属离子,形成保持氧化铈晶型的固溶体结构,但同时调节催化剂表面的酸碱性,并结合催化剂的催化活性,确定催化剂的活性中心。
1 实验部分 1.1 铈基固溶体催化剂制备试剂:硝酸铈、柠檬酸、硝酸镧,分析纯,国药集团化学试剂有限公司;硝酸锌、硝酸镁、硝酸铝,分析纯,天津市风船化学试剂科技有限公司。
铈基固溶体催化剂制备选用柠檬酸做络合剂,其中掺杂金属的物质的量占总物质的量5%,均以金属硝酸盐作为前驱体。首先将金属硝酸盐溶于去离子水中,配成0.2 mol·L-1的溶液。然后将0.2 mol·L-1的柠檬酸溶液缓慢倒入上述盐溶液中。混合溶液在353 K下搅拌3 h后,旋蒸得到油状液体。将旋蒸后的样品置于353 K的烘箱中干燥24 h,然后873 K焙烧5 h,得到铈基固溶体样品。
1.2 催化剂的表征采用日本理学公司的Rigaku D/max-2500射线衍射仪对样品做物相分析。用Cu_Kα 做射线源,工作电流100 mA,工作电压40 kV,扫面速度8(°)/min,扫面角度10°~90°。
采用美国Micromeritics公司的Autochem II 2920化学吸附仪做CO2和NH3吸附。取0.1 g样品,氩气气氛下473 K预处理0.5 h。然后冷却至323 K,利用脉冲吸附CO2和NH3至饱和。再用氩气吹扫除去物理吸附的气体。然后在氦气气氛中10 ℃·min-1程序升温至1 223 K。
1.3 催化剂的活性评价取0.1 g催化剂置于100 mL高压反应釜中,加入15 mL甲醇,反复充气排气排除釜内空气后再充入5 MPa CO2气体。413 K下反应2 h后加正丙醇做内标物用Agilent 4890 D做产物分析。
2 结果与讨论 2.1 催化剂XRD表征对不同掺杂金属的铈基固溶体催化剂进行XRD表征,结果如图 1所示。通过对XRD谱图的分析可以确定Ce1-xMxO2催化剂是否形成固溶体。从图 1看出,掺杂其他金属离子之后,Ce1-xMxO2仍保持着立方萤石结构,并没有出现其他金属氧化物的衍射峰。说明铈与掺杂金属形成了均相混合物。同时观察到虽然Ce1-xMxO2都保持着立方萤石结构,但特征峰的2θ角度都发生了微小的偏移。掺杂Al、Zn和Mg使2θ向高角度偏移,掺杂La使2θ向低角度偏移。

|
| 图 1 不同掺杂金属的Ce1-xMxO2催化剂的XRD图 Fig. 1 XRD patterns of ceria based catalysts with different doping metals |
对应的,它们的晶胞参数也会发生变化,具体数值如表 1所示。
| catalysts | lattice parameter/nm | crystal size/nm |
| CeLaO2 | 0.54361 | 11.0 |
| CeZnO2 | 0.54183 | 13.7 |
| CeMgO2 | 0.54116 | 9.6 |
| CeAlO2 | 0.56245 | 10.1 |
| CeO2 | 0.54194 | 13.1 |
掺杂金属离子导致2θ偏移和晶胞参数变化的原因是Mn+掺杂到CeO2晶格中,使得晶体结构发生变化。Al3+、Mg2+和Zn2+的离子半径小于Ce4+离子半径,当这些离子取代Ce4+时,会使晶格收缩,晶胞参数减少。而La3+离子半径大于Ce4+离子半径,若La3+离子进入氧化铈晶胞中取代Ce4+,会导致晶胞参数增大,这些变化与Lee等[13]报道结果一致,说明形成了Ce1-xMxO2固溶体结构。根据XRD谱图,由谢乐公式计算样品的晶粒大小,从表 1中可以看到掺杂金属离子使催化剂晶粒尺寸都有所减少,但幅度不大。
2.2 催化剂活性评价对不同掺杂金属铈基固溶体催化性能进行了评价,反应条件为:甲醇15 mL,催化剂量0.1 g,413 K下反应2 h。结果如图 2所示。
|
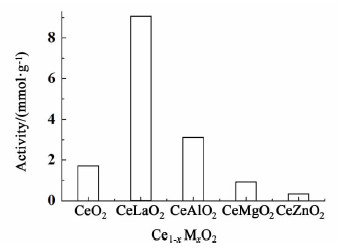
| 图 2 不同掺杂金属铈基固溶体催化性能 Fig. 2 Catalytic performance of Ce1-xMxO2 catalysts. |
从图 2可以看出,掺杂不同金属离子的催化剂活性迥异。纯CeO2的活性为1.72 mmol·g-1,掺杂镧的铈基固溶体活性最高,达到了9.08 mmol·g-1,相当于纯铈样品的5倍。Al的掺杂使得活性略有提高。但是Mg的加入反而使催化性能下降到0.93 mmol·g-1。掺杂Zn的催化剂活性最低,仅有0.34 mmol·g-1。因此,掺杂不同金属离子对氧化铈催化二氧化碳和甲醇合成碳酸二甲酯的活性有不同的影响。接下来,通过BET、CO2-TPD和NH3-TPD考察催化剂活性发生变化的原因。
2.3 铈基催化剂比表面积及孔结构表征对不同催化剂的比表面积和孔结构进行表征,结果如表 2所示。
| catalyst | BET sruface area/(m2·g-1) | pore volume/(cm3·g-1) |
| CeO2 | 36.5 | 0.132 |
| CeLaO2 | 41.2 | 0.131 |
| CeAlO2 | 59.4 | 0.150 |
| CeMgO2 | 41.4 | 0.163 |
| CeZnO2 | 40.6 | 0.116 |
从表 2可以看出,掺杂不同金属离子之后,样品的比表面积都有所增加,其中铈铝固溶体的比表面积最大。样品的孔体积没有太大的变化。结合活性数据发现,催化剂比表面积变化趋势与活性没有直接的关系,说明样品比表面积不是导致催化剂活性发生改变的主要因素。
2.4 催化剂CO2-TPD和NH3-TPD表征图 3和图 4为掺杂不同金属离子铈基固溶体的CO2-TPD和NH3-TPD谱图。

|
| 图 3 不同金属离子掺杂铈基固溶体的CO2-TPD谱图 Fig. 3 CO2-TPD profiles of different doped metals |
|
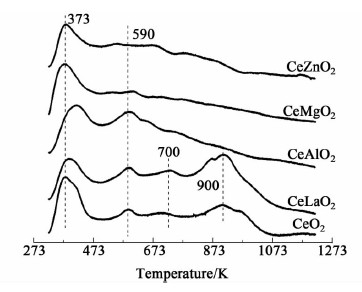
| 图 4 不同金属离子掺杂的铈基固溶体的NH3-TPD谱图 Fig. 4 NH3-TPD profiles of different doped metals |
从图 3可以看出,纯氧化铈在373和590 K出峰,对应的是催化剂表面的弱碱位和中强碱位。掺杂La之后,373 K处弱碱量明显减少,但在700和900 K处有新碱位的出现。掺杂Al的固溶体催化剂,590 K处的峰面积有所增加,但没有强碱位的出现。加入Mg和Zn的催化剂,只有373 K处的弱碱位较为明显,590 K处的中强碱基本消失,且并没有出现700和960 K处的强碱位。
从图 4可看出,纯氧化铈在373、590和900 K处出峰,分别对应催化剂表面的弱酸位、中强酸位和强酸位。当加入La之后,373 K处弱酸位的酸量明显减少,但在700 K处有新峰出现。同时900 K处也有峰出现,但加入La后酸量有明显增加。CeAlO2固溶体在373和590 K处有峰出现,且590 K处峰略有增加。掺杂Mg和Zn之后,590 K处中强酸的峰基本消失,且373 K处的弱酸酸量也有一定的减少。结合样品的活性数据,可以推测:590 K处的中强酸位和碱位以及催化剂表面的强酸强碱位是催化剂的活性中心。因此,CeLaO2活性大幅度提高是因为590 K处的中强酸碱位一直存在,且出现了873~1 073 K之间的强酸碱位。加入Mg和Zn,873~1 073 K处的强酸碱位以及590和700 K处的中强酸碱位均减少甚至消失,导致催化剂活性下降。Al的加入影响比较复杂,虽然没有出现强酸碱位,但在590 K处中强酸碱量略有增加因此活性略有提高。
| [1] | Keller N, Rebmann G, Keller V. Catalysts, mechanisms and industrial processes for the dimethyl carbonate synthesis[J]. Journal of Molecular Catalysis A: Chemical, 2010, 317 (1/2): 1-18 |
| [2] | Wang W, Wang S, Ma X, et al. Recent advances in catalytic hydrogenation of carbon dioxide[J]. Chemical Society Reviews, 2011, 40 (7): 3 703-3 727 |
| [3] | Razali N A M, Lee K T, Bhatia S, et al. Heterogeneous catalysts for production of chemicals using carbon dioxide as raw material: A review[J]. Renewable and Sustainable Energy Reviews, 2012, 16 (7): 4 951-4 964 |
| [4] | Ballivet-Tkatchenko D, Burgat R, Chambrey S, et al. Reactivity of ditert-butyldimethoxystannane with carbon dioxide and methanol: X-ray structure of the resulting complex[J]. Journal of Organometallic Chemistry, 2006, 691 (8): 1 498-1 504 |
| [5] | Jung K. An in situ infrared study of dimethyl carbonate synthesis from carbon dioxide and methanol over zirconia[J]. Journal of Catalysis, 2001, 204 (2): 339-347 |
| [6] | Jung K T, Bell A T. Effects of catalyst phase structure on the elementary processes involved in the synthesis of dimethyl carbonate from methanol and carbon dioxide over zirconia[J]. Topics in Catalysis, 2002, 20 (1): 97-105 |
| [7] | Tomishige K, Ikeda Y, Sakaihori T, et al. Catalytic properties and structure of zirconia catalysts for direct synthesis of dimethyl carbonate from methanol and carbon dioxide[J]. Journal of Catalysis, 2000, 192 (2): 355-362 |
| [8] | Aresta M, Dibenedetto A, Pastore C, et al. Influence of Al2O3 on the performance of CeO2 used as catalyst in the direct carboxylation of methanol to dimethylcarbonate and the elucidation of the reaction mechanism[J]. Journal of Catalysis, 2010, 269 (1): 44-52 |
| [9] | Hofmann H J, Brandner A, Claus P. Direct synthesis of dimethyl carbonate by carboxylation of methanol on ceria-based mixed oxides[J]. Chemical Engineering & Technology, 2012, 35 (12): 2 140-2 146 |
| [10] | Bian J, Xiao M, Wang S J, et al. Graphite oxide as a novel host material of catalytically active Cu-Ni bimetallic nanoparticles[J]. Catalysis Communications, 2009, 10 (11): 1 529-1 533 |
| [11] | Zhou Y, Wang S, Xiao M, et al. Novel Cu-Fe bimetal catalyst for the formation of dimethyl carbonate from carbon dioxide and methanol[J]. RSC Advances, 2012, 2 (17): 6 831-6 837 |
| [12] | La K W, Jung J C, Kim H, et al. Effect of acid-base properties of H3PW12O40/CexTi1-xO2 catalysts on the direct synthesis of dimethyl carbonate from methanol and carbon dioxide: A TPD study of H3PW12O40/CexTi1-xO2 catalysts[J]. Journal of Molecular Catalysis A Chemical, 2007, 269 (1/2): 41-45 |
| [13] | Lee H J, Park S, Song I K, et al. Direct synthesis of dimethyl carbonate from methanol and carbon dioxide over Ga2O3/Ce0.6Zr0.4O2 catalysts: effect of acidity and basicity of the catalysts[J]. Catalysis Letters, 2011, 141 (4): 531-537 |
| [14] | Tomishige K, Furusawa Y, Ikeda Y, et al. CeO2-ZrO2 solid solution catalyst for selective synthesis of dimethyl carbonate from methanol and carbon dioxide[J]. Catalysis Letters, 2001, 76 (1/2): 71-74 |
 2016, Vol. 33
2016, Vol. 33





