2. 天津化学化工协同创新中心, 天津 300072;
3. 天津市功能精细化学品技术工程中心, 天津 300354;
4. 河北君瑞沣新材料有限公司, 河北 衡水 053010
2. Tianjin Chemical and Chemical Collaborative Innovation Center, Tianjin 300072, China;
3. Tianjin Functional Fine Chemicals Technology Engineering Center, Tianjin 300354, China;
4. Hebei Junruifeng New Materials Co. Ltd., Hebei, Hengshui 053010, China
随着国际社会对农药的高效、低毒、低残留和无污染等要求越来越高,以及人们对食品安全意识和环境保护意识的进一步提高,高效、低毒、对环境友好且不易产生抗性的杀虫剂将会得到广泛的应用。苯甲酰基脲类化合物[1, 2]由于其独特的作用机制、较高的环境安全性及广谱高效的杀虫活性等显著优势,已成为创制新农药的一个活跃领域。2,6-二氟苯甲酰基异氰酸酯(简称DFBI)是苯甲酰脲类杀虫剂合成过程中的一个重要中间体,可用于合成几乎所有苯甲酰脲类杀虫剂品种[3-7],如氟铃脲、除虫脲、氟啶脲、氟虫脲、啶蜱脲、氟酰脲、氟苯脲和氟螨脲等。
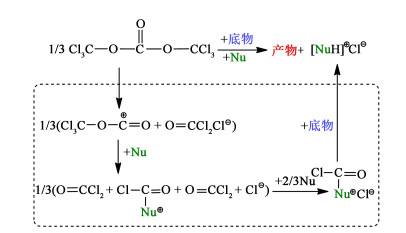
目前DFBI的普遍制备方法是以2,6-二氟苯甲酰胺(简称FBA)为原料,使用光气法[8-10]或者草酰氯法[11-13]合成。除此之外还有Tsuda Akihiko等[14]提出的2,6-二氟-N-(2,2,2-三氯乙酰基)-苯甲酰胺在三乙胺作用下制备DFBI;Zhang等[15]提出的胺与碳酰氟反应制备异氰酸酯;Braverman等[16]提到的2,6-二氟苯甲酰氯和三甲基甲硅烷基异氰酸酯反应;Deng等[17]提出的2,6-二氟苯甲酰氯与氰酸钠反应。由于光气为剧毒气体,贮运具有极大危险性,反应不便计量,因此使用受到限制;草酰氯沸点低,挥发性强,易放出有毒气体,且价格较高。近年新开发的双(三氯甲基)碳酸酯,即三光气(固体光气,简称BTC),常温下为固体,仅为一般有毒物,贮存和使用比气态光气更为安全和方便,1分子BTC可生成3分子的活性中间体(ClCONu+Cl-)[18],在温和条件下它就可以和多种亲核试剂(Nu)进行反应。
从图 1可知,1 mol BTC相当于3 mol光气,是一种理想的光气替代品,BTC在有机化工领域可完全取代光气或双光气实现相关化学品的合成,采用BTC法合成部分苯异氰酸酯类化合物的相关研究引起广泛关注[19-22]。
BTC的使用视具体反应体系而定,当体系中含有引发其分解的物质如有机胺或有机碱时,不需要添加任何引发剂,反应即可顺利进行[24, 25]。本研究以BTC代替光气与FBA进行反应,通过对溶剂、投料方式、反应时间、反应物投料比例以及反应温度进行研究,获得了较适宜合成条件,在此新工艺下可以得到较高的DFBI收率。
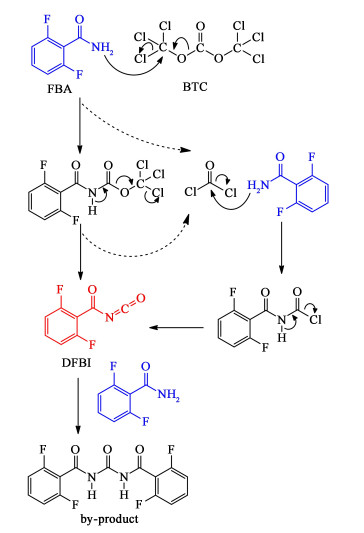
1 实验部分 1.1 实验原理如图 2所示,BTC法合成DFBI反应分为2个阶段:第1阶段为冷光气化反应阶段,FBA与BTC反应生成甲酰基氨基甲酸三氯甲酯和HCl,反应过程中释放出的光气也可与胺反应生成甲酰基氨基甲酰氯和HCl,反应放出大量热量,因此要求反应在低温下进行。反应同时还伴有胺盐酸盐的生成。滴胺速度对反应也产生一定影响,由于反应初期处于放热阶段,滴胺过快会造成反应体系无法及时散热,大量热量积聚,易使副反应发生。
|
| 图 2 BTC法合成DFBI的反应机理 Fig.2 Synthetic mechanism of DFBI by BTC method |
| |
第2阶段为热光气化反应阶段,主要的反应为甲酰基氨基甲酸三氯甲酯和甲酰基氨基甲酰氯分解生成异氰酸酯和HCl,为吸热过程。此外胺盐酸盐可与BTC生成异氰酸酯,并释放出HCl。在反应过程中,胺还可能与异氰酸酯发生副反应生成双缩脲结构,脲类副产物与BTC可继续生成焦油状聚合物。在第2阶段如果保温时间不足,甲酰基氨基甲酸三氯甲酯未充分分解成异氰酸酯,必然会导致收率的降低,甚至得不到产物。但是异氰酸酯在高温下长时间反应会发生自聚,不利于提高产品的纯度和收率,从成本能耗角度考虑也不经济。
1.2 仪器与试剂仪器:低温恒温反应浴;恒温油浴锅;傅里叶变换红外光谱仪;液相色谱仪和400 MHz液体核磁共振谱仪。
试剂:BTC,质量分数为99.5%,平原倍斯特化工有限公司;FBA,质量分数为99.5%,衡水均凯化工有限公司;其它试剂为市售AR。
1.3 实验步骤将0.01 mol(99.5%,2.98 g)BTC和氯苯溶剂加入带有搅拌、温度计以及回流冷凝器的三口瓶中,在-5 ℃下磁力搅拌至BTC完全溶解。将0.03 mol(99.5%,4.74 g)FBA和氯苯混合均匀,经恒压滴液漏斗缓慢滴加到三口瓶中,滴加过程温度在-5~0 ℃,滴加时间30 min,滴加结束后-5 ℃保温搅拌30 min。将三口瓶转移至油浴锅中,缓慢加热1 h至回流,滴加0.01 mol(99.5%,2.98 g)BTC溶液,滴加完毕保持回流状态反应4 h。反应结束后冷却至室温过滤,滤饼经室温氯苯20 mL×3打浆洗涤、电热干燥箱干燥12 h,回收原料FBA,滤液减压蒸馏回收溶剂,得到淡黄色液体产物,通过液相色谱分析定量[柱温30 ℃,流速1 mL ·min-1,检测波长254 nm,流动相V(乙腈) ∶V(水)=70 ∶30,DFBI保留时间约3.6 min],收率为86.4%。
2 结果与讨论 2.1 DFBI的结构表征经红外光谱和核磁共振氢谱、碳谱分析表征并确认了DFBI的分子结构,如图 3所示。

|
| 图 3 目标产物DFBI的结构表征 Fig.3 Structure characterization of DFBI |
| |
DFBI红外结果IR(氯苯,v/cm-1):2 244、1 760、1 625、1 604、1 461、1 295、1 249、1 008、973和794。其中2 244 cm-1为异氰酸酯基(N=C=O)的强吸收峰,酰基的羰基(C=O)吸收峰出现在1 625和1 604 cm-1处。
DFBI核磁结果1H NMR (400 MHz,CD2Cl2) δ:7.69 (tt,J=8.6,6.4 Hz,1H)、7.13 (td,J=8.8,1.3 Hz,2H)。13C NMR (101 MHz,CD2Cl2) δ:164.50、161.95、161.91、135.97、112.29、109.12、92.30、53.40。
2.2 溶剂对产品收率的影响由于原料FBA在不同有机溶剂中溶解度有较大差别,且其溶解效果对反应有影响,固定n(BTC) ∶ n(FBA)=1.0 ∶2.0,BTC分2次均等投料,溶剂用量为100 mL,冷光气化反应阶段-5 ℃反应1 h,在回流条件下反应4 h,考察了不同溶剂对反应的影响,所得结果见表 1。
| 试号 | 溶剂 | 收率/% |
| 1 | 乙酸乙酯 | 24.8 |
| 2 | 乙腈 | 34.0 |
| 3 | 1,2-二氯乙烷 | 41.0 |
| 4 | 氯苯 | 78.7 |
| 5 | 甲苯 | 47.4 |
| 6 | 二甲苯 | 24.2 |
由表 1可知,不同的溶剂反应得到产品的收率不同。乙酸乙酯、乙腈、1,2-二氯乙烷为低沸点溶剂,回流时反应温度较低,导致收率较低;甲苯、二甲苯对原料FBA溶解效果较差,导致收率较低,且容易有副产物生成。所以选用氯苯为反应溶剂。
2.3 BTC投料方式对产品收率的影响由于反应存在冷光气化和热光气化2个反应阶段,相对应的,BTC的投料可分为第1阶段一次投料和两阶段分次投料2种方式。固定n(BTC) ∶n(FBA)=1.0 ∶2.0,冷光气化反应阶段-5 ℃反应1 h,在回流条件下反应4 h,回流温度为124~126 ℃,考察BTC 2种不同的投料方式对反应的影响,所得结果见表 2。
| 试号 | BTC投料方式 | 收率/% |
| 1 | 一次投料 | 72.9 |
| 2 | 二次投料 | 78.7 |
由表 2可知,BTC分2次投料要比一次全加入收率要高,分析原因可能是BTC在反应过程中除了参与反应,还有一部分分解逸出反应体系。一次投料的反应,在反应的前期BTC易分解浪费,而在后期回流过程中BTC浓度不高,反应时间较长,容易发生副反应,导致产物收率降低,所以本实验采取BTC均分两阶段投料的方式。
2.4 反应时间对转化率和收率的影响 2.4.1 第1阶段冷光气化反应固定n(BTC) ∶n(FBA)=1.0 ∶2.0,溶剂为氯苯,BTC分2次均等投料,在回流条件下反应4 h,回流温度为124~126 ℃,考察第1阶段冷光气化(-5 ℃) 反应时间对反应的影响,结果见图 4。
|
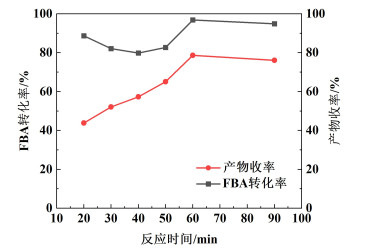
| 图 4 第1阶段反应时间对转化率和收率的影响 Fig.4 Effect of the first-stage reaction time on the conversion and yield |
| |
由图 4可知,第1阶段冷光气化反应时间小于1 h时收率较低,但FBA的转化率却居高不下,其原因可能是反应初期处于放热阶段,滴胺速率过快会造成反应体系无法及时散热,大量热量积聚,易使副反应发生;反应时间大于1 h时收率并没有明显提升,综合收率情况及器材能耗来看第1阶段冷光气化反应时间1 h为最适宜。
2.4.2 第2阶段热光气化反应固定n(BTC) ∶n(FBA)=1.0 ∶2.0,溶剂为氯苯,BTC分2次均等投料,第1阶段冷光气化-5 ℃反应1 h,回流温度为124~126 ℃,考察第2阶段热光气化反应时间对反应的影响,结果见图 5。
|
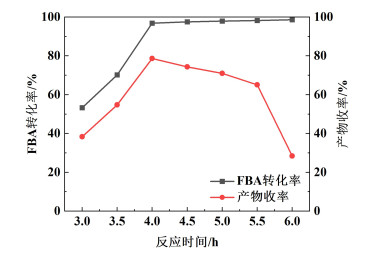
| 图 5 第2阶段反应时间对转化率和收率的影响 Fig.5 Effect of the second-stage reaction time on the conversion and yield |
| |
由图 5可知,第2阶段热光气化反应时间低于4 h时,反应不充分,原料FBA转化率和产物收率都较低;在4 h时产物收率达到最高;随着反应时间增加,副反应也随之增加,原料FBA的转化率变化不大,收率却大幅降低。所以第2阶段热光气化反应回流时间在4 h为最适宜。
2.5 投料物质的量之比对转化率和收率的影响固定溶剂为氯苯,BTC分2次均等投料,第1阶段冷光气化-5 ℃反应1 h,第2阶段热光气化反应时间4 h,反应温度为124~126 ℃,对BTC和原料FBA的投料配比进行了研究,所得结果见图 6。
|
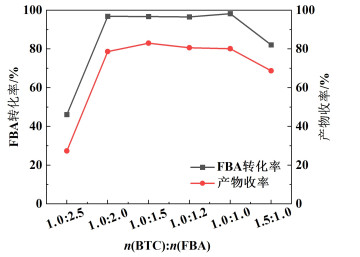
| 图 6 原料投料物质的量之比对转化率和收率的影响 Fig.6 Effect of the molar ratio of raw materials on the conversion and yield |
| |
由图 6可知,当n(BTC) ∶n(FBA)=1.0 ∶2.5时,FBA转化率及产物收率很低,其原因可能是反应溶液中BTC浓度较低,FBA有大量未参与反应,且生成的异氰酸酯产物优先与FBA反应生成副产物脲。随着BTC投料的增加,产物收率也不断增加,当n(BTC) ∶n(FBA)=1.0 ∶1.5时,产物收率达到最大,为83.0%;继续增加BTC的投料,原料FBA转化率及产物收率变化不大。同时由于BTC用量过多将会造成浪费,影响反应的经济效益,所以目前条件下n(BTC) ∶n(FBA)=1.0 ∶1.5可以得到较好的产品收率。
2.6 反应温度对转化率和收率的影响固定n(BTC) ∶n(FBA)=1.0 ∶1.5,溶剂为氯苯,BTC分2次均等投料,第1阶段冷光气化-5 ℃反应1 h,第2阶段热光气化反应时间4 h,考察第2阶段反应回流温度对反应的影响,结果见图 7。
|
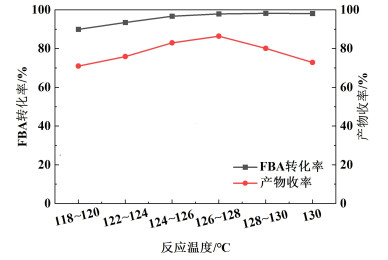
| 图 7 反应温度对转化率和收率的影响 Fig.7 Effect of temperature on the conversion and yield |
| |
由图 7可知,随着反应温度的升高,FBA转化率和产物收率也在不断增加,产物收率在126~128 ℃达到最高86.4%,继续升高反应温度,FBA转化率基本不变,产物收率有所降低。原因可能为温度不高时反应不完全,且反应结束后静置冷却过程中会有少许FBA析出;温度过高时副反应的比例增加,同时液相色谱检测到副产物比例上升,导致产物收率降低。综合来看反应溶剂的回流温度控制在126~128 ℃之间时为最适宜。
2.7 未反应FBA的回收套用虽然FBA转化率比较高,但是仍然有少部分未转化,将其回收套用,可降低生产成本。在投料物质的量之比n(BTC) ∶n(FBA)=1.0 ∶1.5,溶剂为氯苯,BTC分2次均等投料,低温-5 ℃反应1 h,回流反应时间4 h,反应回流温度126~128 ℃的条件下,反应结束后冷却、减压蒸馏回收溶剂,得到淡黄色液体产物DFBI。由于FBA在产物中的溶解度很低,将液体产物在5 ℃冷却静置,有白色结晶析出,过滤分离出液体产物,将固体结晶洗涤干燥回收,经高效液相色谱分析证明为原料FBA。FBA的回收结果见表 3。
| 试号 | FBA转化率/% | 产物收率/% | FBA回收率/% | w(FBA)/% |
| 1 | 94.9 | 84.3 | 4.5 | 97.4 |
| 2 | 95.5 | 86.4 | 3.6 | 97.7 |
| 3 | 95.0 | 84.7 | 4.2 | 97.3 |
| 4 | 95.1 | 85.4 | 4.0 | 98.4 |
由表 3中数据可知,FBA的转化率与FBA的回收率合计均在99%以上,表明未参与反应的FBA基本都可以回收,其质量分数也达到97%以上。产物收率稍低的原因主要在于生成了如图 2中所示脲类副产物,经高效液相色谱分析该副产物在产物中含量约为10%,未来进一步提高产品收率需有效提高反应选择性,如何更好地抑制该副反应将是工艺研发的重点方向。
将回收的FBA重新投料,与BTC在最适宜条件下进行反应,FBA转化率为95.6%,产物收率为84.8%,证明回收的FBA质量较好,可以循环套用,由于FBA价格高于BTC,对FBA的回收再利用具有更高的经济效益。
3 结论(1) 以FBA和BTC为原料进行反应,可以有效生成苯甲酰基脲类农药中间体DFBI,通过系统的实验研究确定了反应的较适宜工艺条件:投料n(BTC) ∶ n(FBA)=1.0 ∶1.5,溶剂为氯苯,BTC分2次均等投料,冷光气化阶段低温-5 ℃反应1 h,热光气化阶段在126~128 ℃回流反应4 h,产品收率达到86.4%,原料FBA转化率95.5%。少量未反应的原料FBA可以进行回收,在上述反应条件下,回收的FBA转化率为95.6%,产物收率为84.8%,证明回收的FBA质量较好,可以循环套用。
(2) 本研究所开发工艺采用BTC代替光气进行反应,具有工艺条件温和,操作简单安全的优点,更加符合绿色化学的要求,具有较好的社会效益和经济效益,适合工业化应用。
| [1] |
王燕燕. 苯甲酰脲类杀虫剂研究进展[J]. 广东化工, 2021, 48(19): 102-103. WANG Yanyan. Research progress of benzoylurea insecticides[J]. Guangdong Chemical Industry, 2021, 48(19): 102-103. (in Chinese) |
| [2] |
张婧, 黄治强, 王丹婷, 等. 苯甲酰脲类杀虫剂在农药复配物中的应用进展[J]. 农药, 2015, 54(10): 703-708, 723. ZHANG Jing, HUANG Zhiqiang, WANG Danting, et al. Application of benzoylurea insecticides in pesticidal composition[J]. Agrochemicals, 2015, 54(10): 703-708, 723. (in Chinese) |
| [3] |
刘安昌, 余彩虹, 张树康, 等. 新型杀虫剂双三氟脲的合成[J]. 武汉工程大学学报, 2015, 37(1): 11-13. LIU Anchang, YU Caihong, ZHANG Shukang, et al. Synthetic process of novel pesticides Bistrifluron[J]. Journal of Wuhan Institute of Technology, 2015, 37(1): 11-13. (in Chinese) |
| [4] |
陈华, 彭彩群, 潘光飞, 等. 杀虫剂氟啶脲的合成[J]. 精细化工中间体, 2013, 43(2): 20-21. CHEN Hua, PENG Caiqun, PAN Guangfei, et al. Synthesis of insecticide chlorfluazuron[J]. Fine Chemical Intermediates, 2013, 43(2): 20-21. (in Chinese) |
| [5] |
SUN R, ZHANG Y, BI F, et al. Design, synthesis, and bioactivity study of novel benzoylpyridazyl ureas[J]. Journal of Agricultural and Food Chemistry, 2009, 57(14): 6356-6361. DOI:10.1021/jf900882c |
| [6] |
黄治强, 张婧, 王丹婷, 等. 含有氨基甲酸酯基结构的苯甲酰脲类化合物及制备方法和杀虫应用: CN105085326B[P]. 2017-04-19 HUANG Zhiqiang, ZHANG Jing, WANG Danting, et al. Benzoyl urea compound containing urethane group structure as well as preparation method and insecticidal application of benzoyl urea compound: CN105085326B[P]. 2017-04-19 (in Chinese) |
| [7] |
SUN R, WANG Z, LI Y, et al. Design, synthesis, and insecticidal evaluation of new benzoylureas containing amide and sulfonate groups based on the sulfonylurea receptor protein binding site for diflubenzuron and glibenclamide[J]. Journal of Agricultural and Food Chemistry, 2013, 61(3): 517-522. DOI:10.1021/jf304468b |
| [8] |
SCHERER O, HORLEIN G, SCHONOWSKY H. Urea derivatives and their use as herbicides: US4013452[P]. 1977-03-22
|
| [9] |
魏红涛, 谭效松, 田德美, 等. 苯甲酰异氰酸酯合成路线及反应条件研究[J]. 湖南化工, 2000, 30(5): 17-19. WEI Hongtao, TAN Xiaosong, TIAN Demei, et al. Studies on the preparation of benzoyl isocyanates[J]. Hunan Chemical Industry, 2000, 30(5): 17-19. (in Chinese) |
| [10] |
曾益良, 宋建军, 张平南, 等. 取代苯甲酰脲类昆虫生长调节剂的合成方法: CN1580042A[P]. 2005-02-16 ZENG Yiliang, SONG Jianjun, ZHANG Pingnan, et al. Substituted benzoyl urea insect growth regulator synthesizing method: CN1580042A[P]. 2005-02-16 (in Chinese) |
| [11] |
BALICKI R, SOBOTKA W, EJMOCKI Z. Insect chitin formation inhibitors. Part Ⅳ. Synthesis of novel 3-substituted 1-(2,6-dihalobenzoyl)urea derivatives[J]. Polish Journal of Chemistry, 1991, 65(5-6): 1049-1053. |
| [12] |
刘强, 曹桂荣, 魏文珑, 等. 异氰酸酯化合物的研究进展[J]. 山西化工, 2007, 27(5): 28-32, 43. LIU Qiang, CAO Guirong, WEI Wenlong, et al. Research progress of isocyanates[J]. Shanxi Chemical Industry, 2007, 27(5): 28-32, 43. (in Chinese) |
| [13] |
王明慧, 许良忠, 苏龙杰, 等. 一种含氟苯甲酰脲苯并咪唑类化合物及其应用: CN103864694A[P]. 2014-06-18 WANG Minghui, XU Liangzhong, SU Longjie, et al. Fluorine-containing benzoylurea benzimidazole compound and application thereof: CN103864694A[P]. 2014-06-18 (in Chinese) |
| [14] |
TSUDA A, OKAZOE T, WADA H, et al. Method for producing N-substituted trihaloacetamide: WO2020196553[P]. 2020-10-01
|
| [15] |
张妮, 贾晓卿, 庆飞要. 一种使用胺与碳酰氟制备异氰酸酯的方法: CN106631899B[P]. 2018-12-18 ZHANG Ni, JIA Xiaoqing, QING Feiyao. Method for preparing isocyanate by using amine and carbonyl fluoride: CN106631899B[P]. 2018-12-18 (in Chinese) |
| [16] |
BRAVERMAN S, CHERKINSKY M, BIRSA M L. Carbon dioxide, carbonyl sulfide, carbon disulfide, isocyanates, isothiocyanates, carbodiimides, and their selenium, tellurium, and phosphorus analogues[J]. ChemInform, 2005, 36(38). |
| [17] |
DENG M, CAUBERE P, SENET J P, et al. Condensation of acyl chloride on sodium cyanate: Preparation of acyl isocyanates[J]. Tetrahedron, 1988, 44(19): 6079-6086. |
| [18] |
赵晓霞, 史宝萍, 李兴, 等. 固体光气的性质及应用研究进展[J]. 化工时刊, 2010, 24(5): 67-73. ZHAO Xiaoxia, SHI Baoping, LI Xing, et al. A review of the properties and application of solid phosgene[J]. Chemical Industry Times, 2010, 24(5): 67-73. (in Chinese) |
| [19] |
毛丽萍, 王伟, 王东亮, 等. 苯二亚甲基二异氰酸酯生产过程专利技术分析[J]. 应用化工, 2020, 49(11): 2926-2931. MAO Liping, WANG Wei, WANG Dongliang, et al. Analysis of China patent technology for xylylene diisocyanate production[J]. Applied Chemical Industry, 2020, 49(11): 2926-2931. (in Chinese) |
| [20] |
刘士民, 王培学, 邓友全. 非光气制异氰酸酯绿色过程[J]. 中国科学: 化学, 2020, 50(2): 235-244. LIU Shimin, WANG Peixue, DENG Youquan. Green non-phosgene process for manufacturing isocyanates[J]. Scientia Sinica Chimica, 2020, 50(2): 235-244. (in Chinese) |
| [21] |
唐文涛, 帅棋. 双(三氯甲基)碳酸酯在药物合成应用中的新进展[J]. 浙江化工, 2017, 48(5): 20-22. TANG Wentao, SHUAI Qi. Recent applications of bis(trichloromethyl) carbonate in drug synthesis[J]. Zhejiang Chemical Industry, 2017, 48(5): 20-22. (in Chinese) |
| [22] |
GANIU M O, NEPAL B, VAN HOUTEN J P, et al. A decade review of triphosgene and its applications in organic reactions[J]. Tetrahedron, 2020, 76(47): 131553. |
| [23] |
季宝, 翟现明, 许毅. 三光气的反应机理和应用[J]. 科技情报开发与经济, 2009, 19(10): 136-137. JI Bao, ZHAI Xianming, XU Yi. The reaction mechanisms and application of triphosgene[J]. Sci-Tech Information Development & Economy, 2009, 19(10): 136-137. (in Chinese) |
| [24] |
刘立芬, 徐德志, 陈欢林, 等. 5-异氰酸酯-异肽酰氯的合成[J]. 化工进展, 2013, 32(1): 184-187, 198. LIU Lifen, XU Dezhi, CHEN Huanlin, et al. Synthesis of 5-isocyanato-isophthaloyl chloride[J]. Chemical Industry and Engineering Progress, 2013, 32(1): 184-187, 198. (in Chinese) |
| [25] |
齐庆莹. 固体光气法合成3, 4-二甲氧基苯异氰酸酯[J]. 精细化工中间体, 2008, 38(2): 35-37. QI Qingying. Synthesis of 3, 4-dimethoxyphenylisocyanate using triphosgene[J]. Fine Chemical Intermediates, 2008, 38(2): 35-37. (in Chinese) |
 2024, Vol. 41
2024, Vol. 41